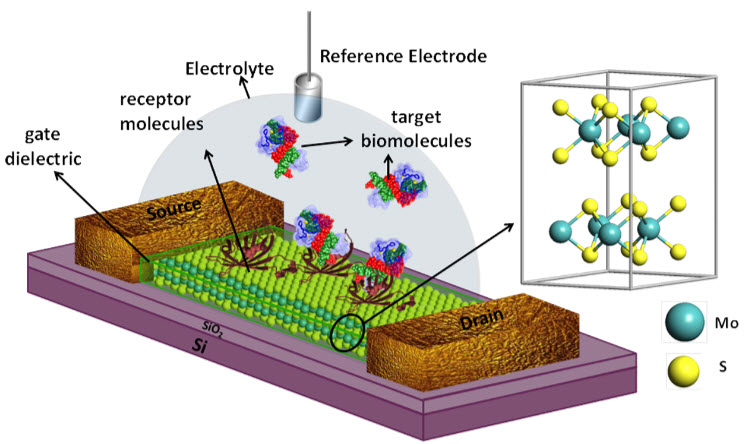
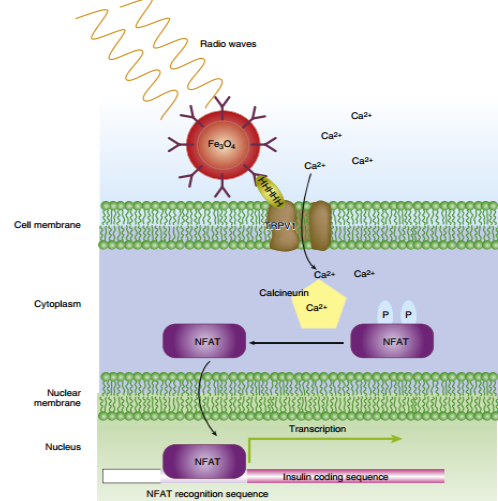
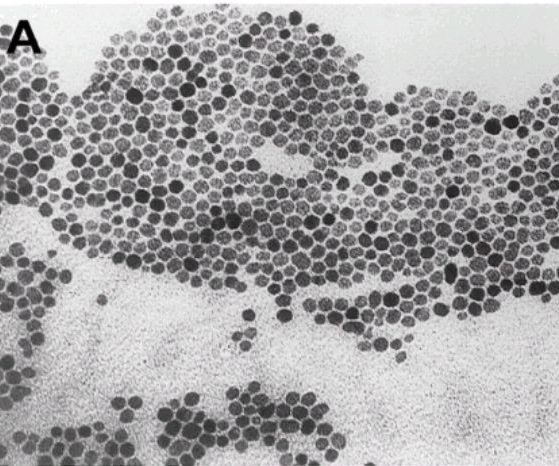
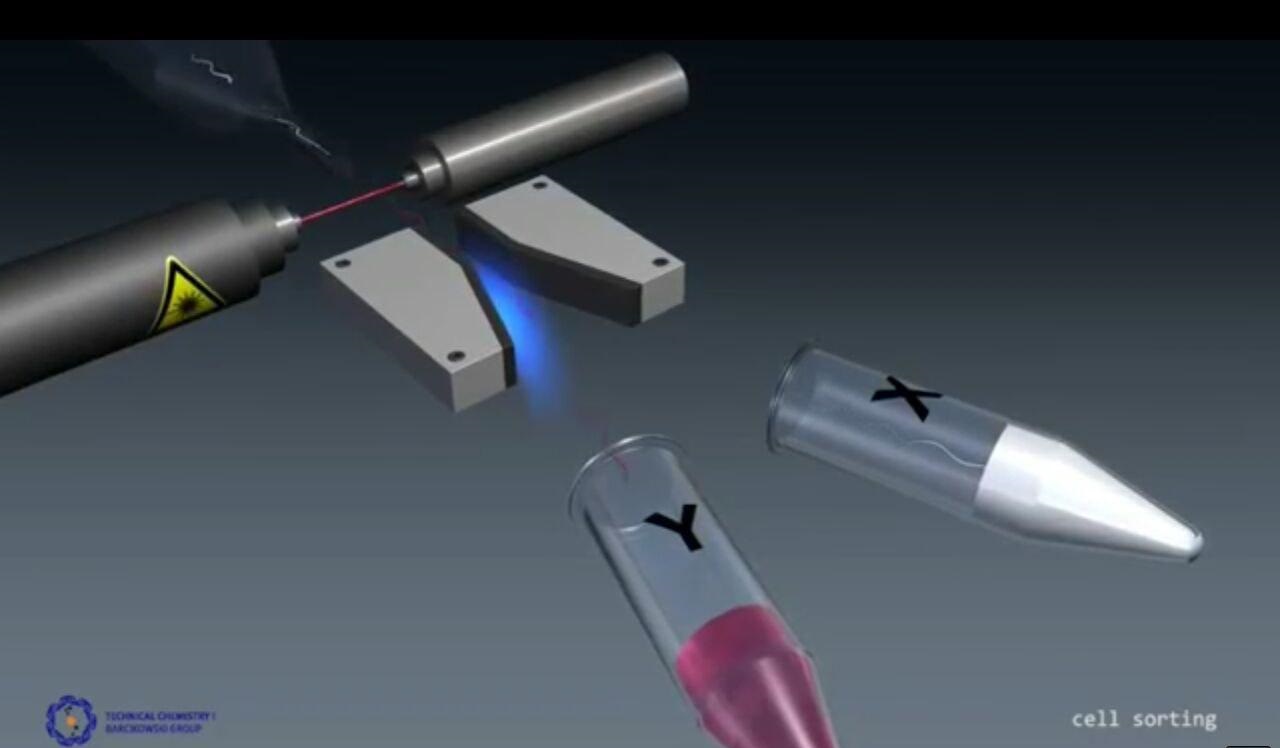
رابط های مغزی، عیوب انسانی را می پوشانند. اطلاعات بیشتر در صفحات اجتماعی بیوتکر
Edit Content
درباره ما
بیوتکر سفیر ترویج زیست فناوری و مرجع دانستی های بیوتکنولوژی. اینجا با هم کلی کتاب و مقاله علمی با موضوعات جذاب می خونیم
با ما تماس بگیرید
- تهران، میدان انقلاب، خیابان کارگر شمالی
- 09367305950
- saeedkargar@gmail.com
- ساعات کاری : شنبه تا جمعه (8 صبح تا 10 شب)