
اصول کلی روش الکتروفورز (Electrophoresis)
(Electrophoresis) الکتروفورز :
الکتروفورز یکی از تکنیکهاي آنالیتیکی قدرتمند در جداسازي و آنالیز دامنه وسیعی از آنالیتهاي یونیزه محسوب میگردد. آنالیتهایی که بطور ویژه مورد توجه قرار میگیرند عبارتند از: پروتئینها , پپتیدها , آمینواسیدها , اسیدهاي نوکلئیک و اولیگونوکلئوتیدها , نوکلئوزیها , اسیدهاي آلی و آنیونها و کاتیونهاي کوچک موجود در مایعات و بافتهاي بدن. اصطلاح الکتروفورز اشاره به حرکت همه ترکیبات یا ذرات باردار در یک محلول (محیط مایع) تحت تاثیر جریان الکتریکی دارد.
ترکیبات شیمیایی داراي بار الکتریکی به سمت قطب آند و یا کاتد (با توجه به نوع بار الکتریکی) حرکت ترکیباتی هستند که وابسته به نوع محیط (قلیایی بودن یا اسیدي بودن) (Ampholytes) مینمایند. آمفولیتها میباشند و نیز –NH2 , -COOH داراي بار منفی یا بار مثبت میباشند. از آنجایی که پروتئینها حاوي گروههاي بارهاي موجود در اسیدهاي نوکلئیک میتوانند به صورت مثبت و یا منفی باشند , در محلولها داراي رفتاري مشابه رفتار آمفولیتها میباشند.
سرعت حرکت ترکیبات موجود در یک نمونه در الکتروفورز به عوامل زیر وابسته است:
1. بار الکتریکی خالص یون .
2. اندازه و شکل یون .
3. شدت میدان الکتریکی.
4. خواص محیط پایه (Support medium)
5. دماي محیط الکتروفورزي.
حرکت الکتروفورزي (μ) :
برحسب تعریف عبارت است از میزان حرکت ذرات برحسب cm/s در واحد میدان الکتریکی برحسب Volt/cm که با μ نشان داده میشود و برحسب cm2/V.s بیان میگردد:
حرکت الکتروفورزي : μ
بار الکتریکی خالص یون : Q
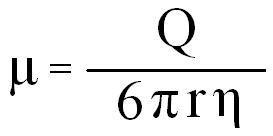
شعاع یون : r
ویسکوزیته محیط(بافر) : η
بطورکلی نیروهاي تاثیر گذارنده بر حرکت الکتروفورزي را میتوان به دو گروه تقسیم نمود:
نیروي رانشی یا جلوبرنده (Driving force) : که مرتبط با میدان الکتریکی یون مربوطه میباشد.
نیروي بازدارنده (Retarding force) : که مربوط به مقاومت محیط نگهدارنده میباشد.
با توجه به معادله بالا مشخص میگردد که حرکت الکتروفورزي ارتباط مستقیم با بار خالص یون(Q) و ارتباط معکوس با اندازه ملکول (r) و ویسکوزیته محیط الکتروفورزي (η) دارد. هنگامی که الکتروفورز در حال انجام میباشد به مرور دماي محیط پایه و بافرها افزایش مییابد که منتج به تبخیر حلال میگردد, این اثر (خشک کنندگی) سبب صعود بافر از هردو بخش بافري(درون دو تانک بافري) به درون محیط پایه میگردد, این جریان دوطرفه بر حرکت یونها تاثیر میگذارد (Wick flow).
مقاله مرتبط :
جزوه ژل الکتروفورز ژل آگارز همراه با فیلم آموزشی (فارسی)
کلیپ آموزشی ژل الکتروفورز
کلیپ قالب گیری ژل الکتروفورز
وسایل و مواد مورد نیاز الکتروفورز :
یک دستگاه (سیستم) الکتروفورز شامل بخشهاي زیر میباشد:
دو تانک بافر (Buffer boxes) که بافرهاي الکتروفورزي در آن ریخته میشود
الکترودها
محیط پایه الکتروفورزي (Support media)
صفحه پوشاننده (Cover) جهت جلوگیري از تبخیر
سیستم تامین کننده جریان الکتریکی (Power supply)
بافر(تامپون)
محیط پایه الکتروفورزي (Support media)

محیط پایه الکتروفورزي (Support media) :
ژل نشاسته نخستین ژلی بود که براي جداسازي الکتروفورزي استفاده گردید. در حال حاضر از آگارز , استات سلولز و پلیآکریلامید استفاده میگردد.
ژل آگارز (Agarose) :
آگار پلی ساکارید اسیدي کمپلکسی میباشد که محتوي منومرهایی از گالاکتوز سولفاته میباشد. آگارز در واقع همان آگاري میباشد. آگارز در واقع همان آگاري میباشد که فاقد گروه سولفات میباشد. ناخالصی در آگارز و وجود آگار و آگاروپکتین(که داراي گروههاي سولفات و کربوکسیلیک اسید میباشند) موجب اختلال در حرکت ملکولها و نیز در رنگآمیزي میگردد ولی در آگارز خالص به دلیل اینکه گروههاي قابل یونیزه مذکور وجود ندارد , کارایی بهتري در جداسازي ترکیبات به روش الکتروفورز (نسبت به ترکیبات مذکور) دارد. از لحاظ عملی محلولهاي بافر حاوي 0.5 تا 1 gr/dL آگارز، ایجاد کننده ژلی با قدرت یونی مناسب براي جداسازي پروتئینها و قطعات DNA با طول 0.5 تا 20 هزار جفت باز می باشد.
اندازه حفره موجود در ژل , بستگی به غلظت آگارز در بافر دارد. هر باند تفکیک شده حاوي چندین پروتئین با حرکت الکتروفورزي یکسان میباشد. در این نوع از محیطهاي الکتروفورزي , باندها بیشتر به صورت پهن دیده می شوند زیرا ژل آگارز نسبت به محیطهاي دیگر مانند استات سلولز نسبت پروتئینها از نفوذپذیري بالایی برخوردار میباشد.
استات سلولز :
کاغذها بیشتر از جنبه جداسازي ترکیبات با وزن ملکولی پایین حائز اهمیت میباشند. مزیت اصلی این محیطها نازك بودن و قدرت مکانیکی آنهاست. این محیطها داراي حساسیت بیشتري میباشند زیرا به نمونه کمتري براي ایجاد لکه ها یا باندهاي قابل تشخیص دارند. کاغذ استات سلولز از جمله این محیطهاست. استات سلولز بوسیله قرار دادن کاغذ سلولز در مجاورت انیدرید استیک ایجاد میگردد. گروه استیل بر روي گروههاي هیدروکسیل قند قرار میگیرد.
ژل پلی آکریلامید :
از پلیمریزاسیون آکریلامید در حضور حرارت ایجاد میگردد که ممکن است داراي پیوندهاي متقاطع یا فاقد باشد. ژل پلیآکریلامید پایدار در برابر حرارت بوده و شفاف میباشد و همچنین (Cross link) پیوندهاي متقاطع فاقد بار الکتریکی میباشد به همین دلیل تداخلی که در ژل آگارز وجود داشت در اینجا وجود ندارد. به علت خاصیت کارسینوژنیک (سرطانزایی) آکریلامید , باید توجه داشت که این ترکیب با سطح پوست برخورد نداشته باشد. ژل پلی متیلن بیس آکریلامید(بیس آکریلامید) شکل میگیرد. – N,N آکریلامید از ترکیب آکریلامید و یک ماده رابط بنام بدین صورت که ملکولهاي آکریلامید بصورت طولی به هم متصل میگردند و ماده رابط نیز مسئول تولید پلهاي عرضی متعدد بین رشته هاي آکریلامید است. خصوصیات فیزیکی ژل از قبیل اندازه منافذ , خاصیت الاستیکی , چگالی ژل و قوام مکانیکی متاثر از غلظت دو جزء تشکیل دهنده آن است. پلیمریزاسیون آکریلامید یک واکنش
رادیکالی است که توسط پراکسیداز یا انرژي فتوشیمیایی شروع میشود.
بافرها:
اعمال بافرها در فرایند الکتروفورز عبارت است از:
1. عبور دادن جریان الکتریکی
2. ثابت نگه داشتن pH محیط
3. تعیین بار الکتریکی سطح ترکیب موجود در نمونه
از عوامل بسیار اساسی در الکتروفورز pH نوع بافر و خصوصیات آن از قبیل قدرت یونی , ظرفیت بافري و معین و قدرت یونی خاص صورت میگیرد.جداسازي ملکولها در الکتروفورز در یک pH محسوب میگردد.
رنگ آمیزي ژلهاي الکتروفورزي (Staining) :
رنگ آمیزي ژلها (محیطهاي پایه)ي الکتروفورزي جهت آشکار شدن جایگاه باندهاي پروتئین و … صورت میگیرد. انتخاب رنگها با توجه به نوع ژل و نوع ترکیب مورد جداسازي صورت میگیرد. میزان رنگ هر باند با میزان پروتئین موجود در آن باند ارتباط دارد ولی این میزان تحت تاثیر عوامل دیگري نظیر نوع پروتئین و میزان دناتوراسیون آن قرار میگیرد. وقتی از رنگ آمیزي پروتئینها استفاده میشود بخش لیپیدي لیپوپروتئین ها یا کربوهیدراتی گلیکوپروتئین ها رنگ نمیشود. لذا مقادیر آنها کمتر از میزان واقعی برآورد خواهد شد.
رنگ آمیزي پروتئین ها :
از رنگهاي آمیدوبلاك (Amido black)، کوماسی بریلیانت بلو (CBB)، پانسو S (Panseau S) و نیترات نقره استفاده می شود.
رنگ آمیزي لیپوپروتئین ها :
از رنگهاي سودان بلاك، کوماسی بریلیانت بلو (CBB) و Oil Red 0 استفاده می شود.
رنگ آمیزي گلیکوپروتئین ها :
از رنگ Periodic Acid Schiff یا (PAS) استفاده می شود.
رنگ آمیزي اسیدهاي نوکلئیک :
استفاده از اتیدیوم بروماید (Ethidium bromide) و نیترات نقره
رنگ آمیزي دهیدروژنازها :
استفاده از NADH (داراي خاصیت فلوئورسان) و نمک تترازولیوم (نیتروبلوتترازولیوم)
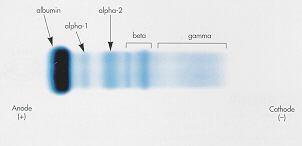
تشخیص و تعیین کمی اجزاي باندهاي تشکیل شده :
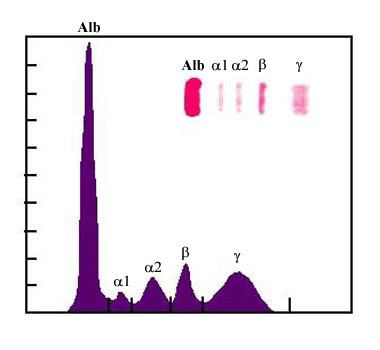
معمولترین روش تعیین مقدار اجزاي باندهاي الکتروفورزي, چگالی سنجی یا دانسیتومتري است (به دستگاه مزبور نیز دانسیتومتر (Densitometry) گفته میشود که به عنوان یک فتومتر فیلتردار و وسیله رسم منحنی محسوب میگردد) که در آن از باندهاي مختلف یک محیط الکتروفورتیک شفاف (فاقد رنگ زمینه اي) و ثابت شده, اسکن تهیه و این اسکن به صورت توالی از قله هاي مجزا , به نام الکتروفورتوگرام نمایش داده میشود.
سطح منحنی زیر این قلهها متناسب با غلظت پروتئینهاي موجود در هر باند میباشد. براي مثال, به این طریق میتوان درصد پروتئینهاي موجود در هر کدام از باندهاي الکتروفورتیک پروتئینهاي سرم را بدست آورد. با ضرب کردن این درصدها در میزان تام پروتئینهاي سرم, غلظت هر باند محاسبه میگردد (شکل زیر).
انواع روشهاي الکتروفورزي
بسته به اینکه الکتروفورز در یک سطح افقی انجام گیرد یا در یک سطح عمودي به ترتیب به نوع روشهاي مذکور
الکتروفورز افقی و الکتروفورز عمودي گفته میشود. از سوي دیگر براساس نوع محیط پایه و مواد شیمیایی مورد
استفاده و همچنین نوع مکانیسم جداسازي, روشهاي الکتروفورزي تنوع زیادي پیدا کردهاند. ازجمله میتوان انواع زیر
را نام برد:
الکتروفورز بر روي ژل آگارز (Agarose Gel Electrophoresis or AGE)
الکتروفورز بر روي استات سلولز (Cellulose Acetate Electrophoresis or CAE)
الکتروفورز بر روي ژل پلی آکریلامید (Polyacrylamide Gel Electrophoresis or PAGE)
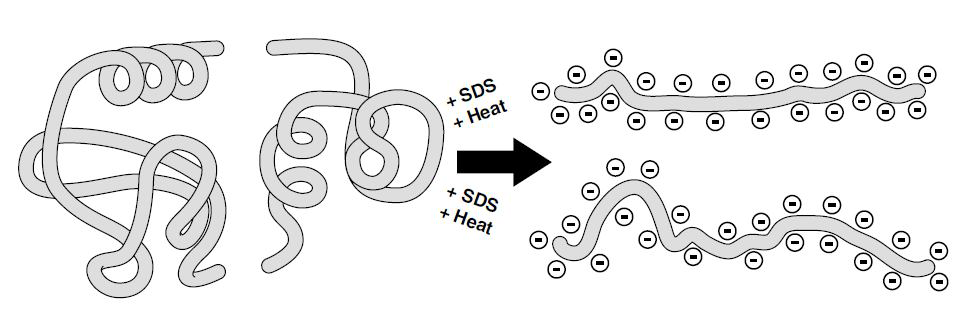
روش SDS-PAGE
که همان روش PAGE می باشد بعلاوه اینکه در اینجا از یک دترژانت به نام سدیم دو دسیل سولفات یا SDS استفاده میگردد که باعث اتصال به سطح ترکیباتی مانند پروتئین ها گردیده و باعث ایجاد بار منفی بر سطح همه آنها میگردد (شکل پایین). میزان بار منفی تشکیل شده بر سطح پروتئینها به اندازه و وزن ملکولی آنها بستگی دارد, بنابراین جداسازي در این روش بر اساس وزن ملکولی ترکیبات صورت خواهد گرفت).
ایزوالکتریک فوکوسینگ (Isoelectric focusing or IEF) – که در این روش از محیط الکتروفورزي با گرادیانی(شیبی) از pH استفاده میگردد که پروتئین ها براساس pH ایزوالکتریکشان جداسازي میگردند.



