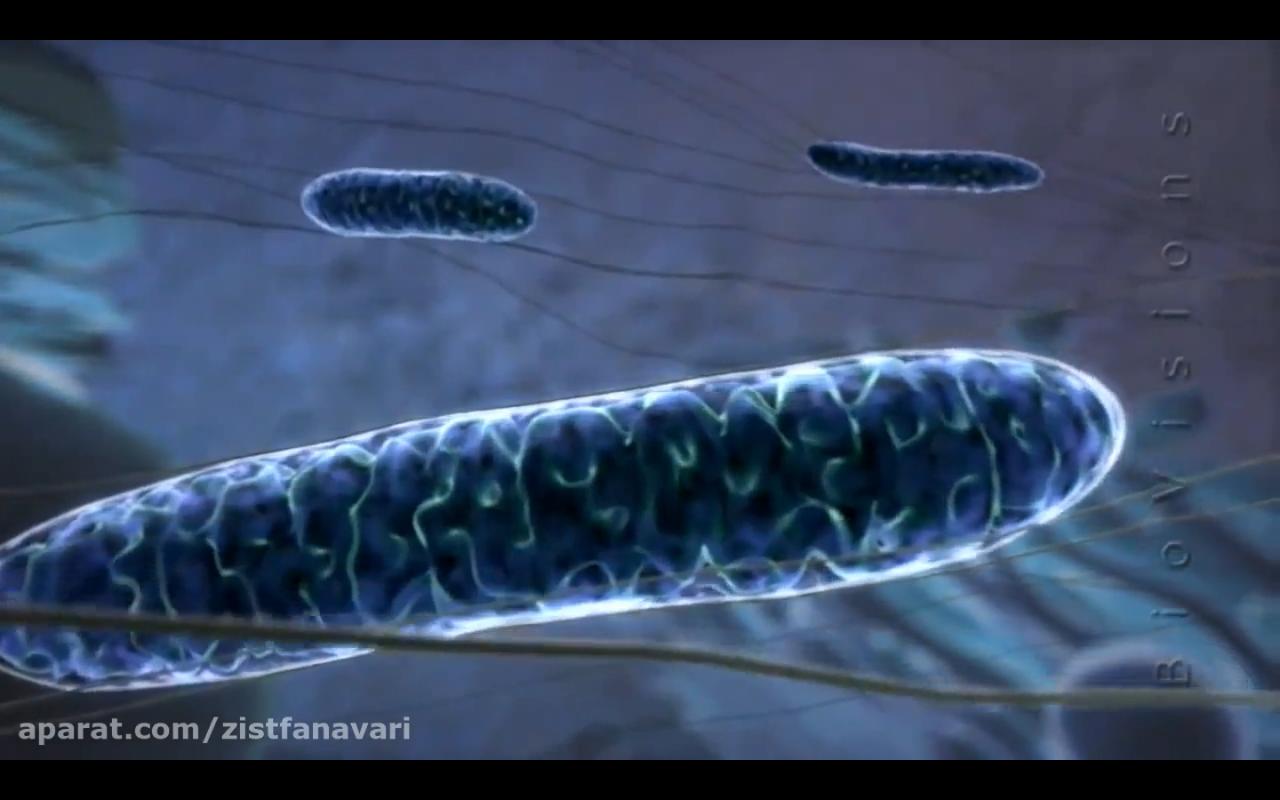
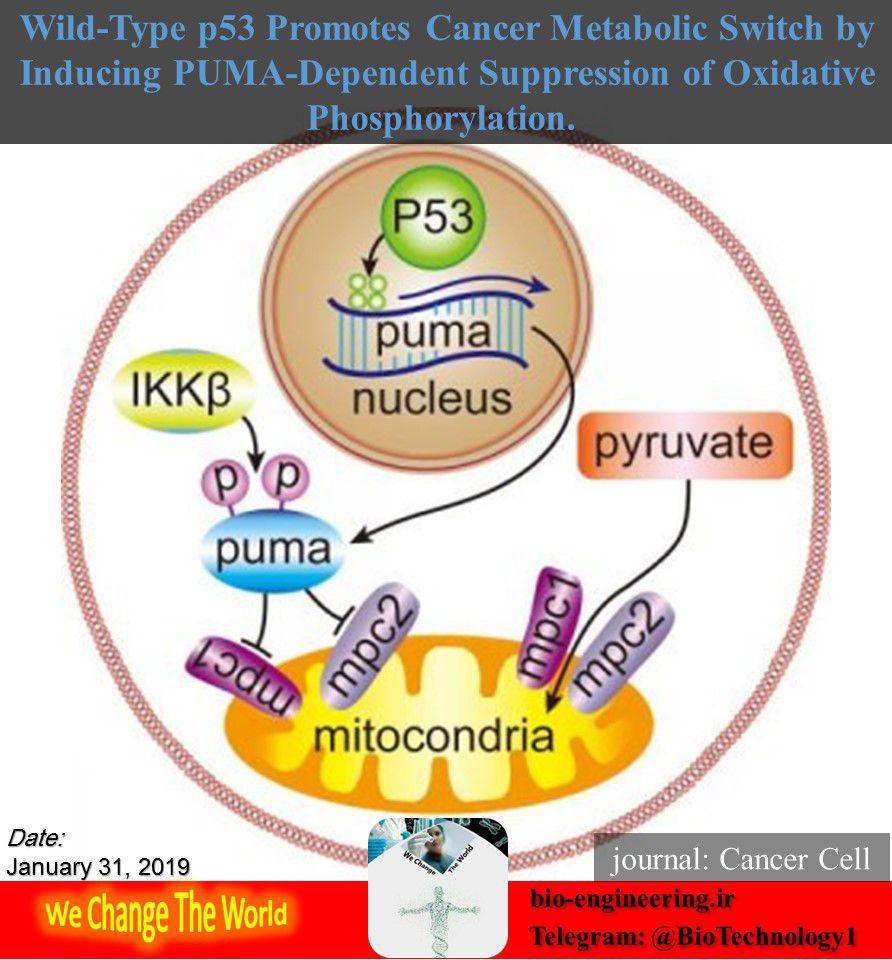
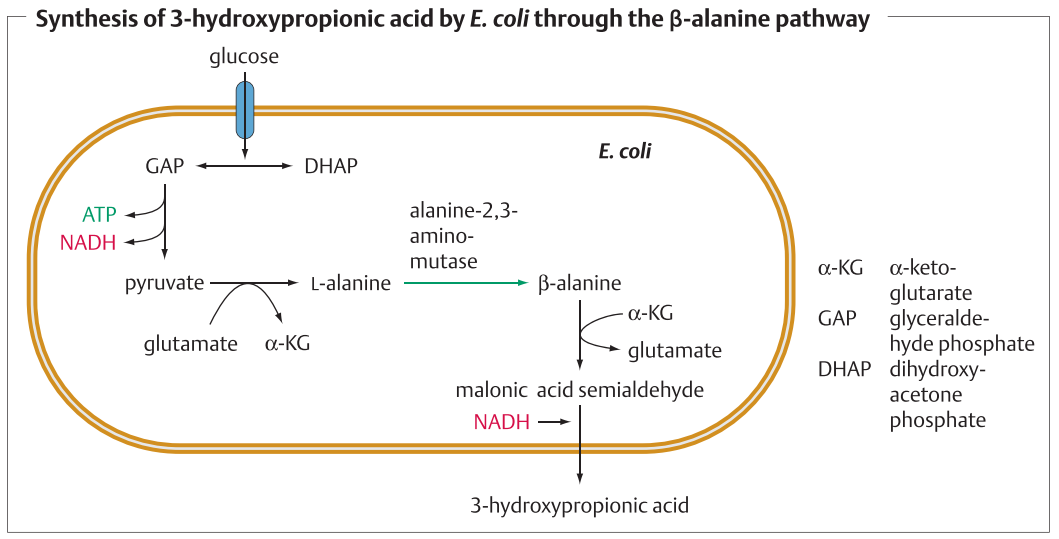
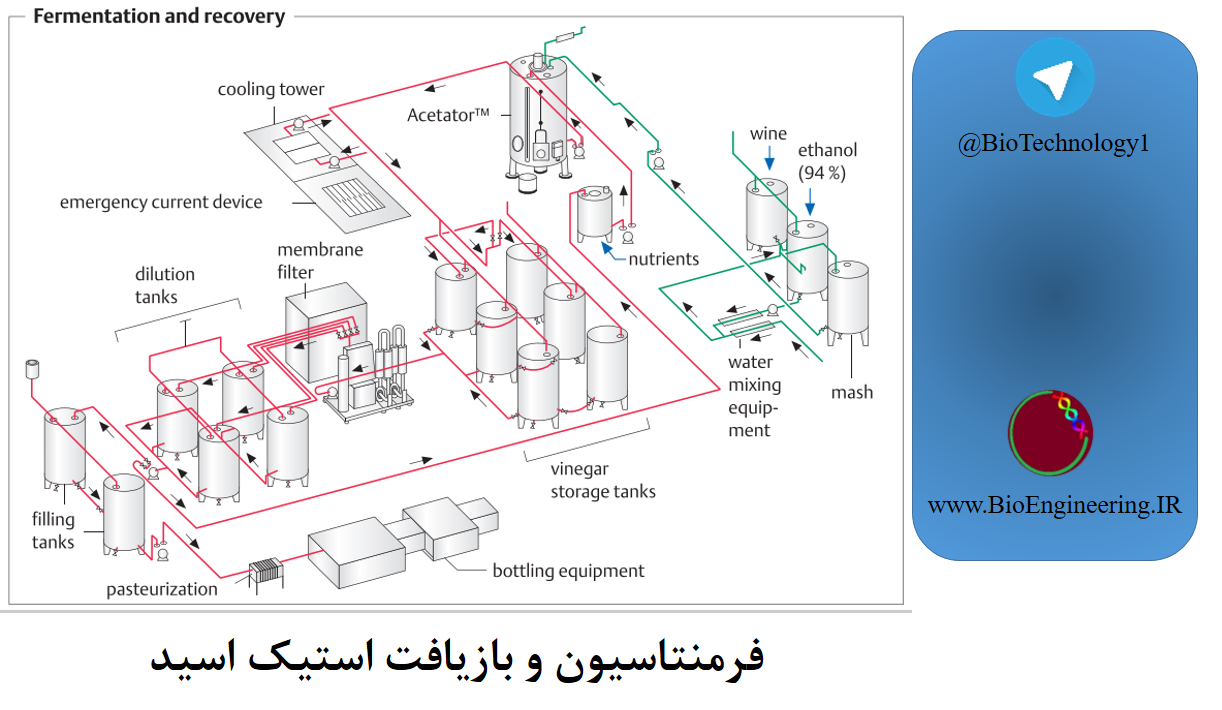
راکیزه یا میتوکندری (به انگلیسی: Mitochondrion) در یاخته (سلول)، اندامکی است که وظیفه آن تنفس سلولی و نوعی اندامک انتقال انرژی است که موجب میشوند انرژی شیمیایی موجود در مواد غذایی با عمل فسفوریلاسیون اکسیداتیو، به صورت پیوندهای پرانرژی فسفات…
درباره ما
بیوتکر سفیر ترویج زیست فناوری و مرجع دانستی های بیوتکنولوژی. اینجا با هم کلی کتاب و مقاله علمی با موضوعات جذاب می خونیم
با ما تماس بگیرید
- تهران، میدان انقلاب، خیابان کارگر شمالی
- 09367305950
- saeedkargar@gmail.com
- ساعات کاری : شنبه تا جمعه (8 صبح تا 10 شب)